Хімія. 9 клас. Ярошенко
Цей підручник можна завантажити у PDF форматі на сайті тут.
§ 42. Завдання різних рівнів складності з теми «Найважливіші органічні сполуки»
1. Установіть відповідність між назвою та формулою вуглеводнів.
|
Назва |
Формула |
||
|
1 |
метан |
А |
С2Н2 |
|
2 |
етен |
Б |
С2Н4 |
|
3 |
етан |
В |
С2Н6 |
|
4 |
етин |
Г |
СН4 |
|
Д |
С6Н6 |
||
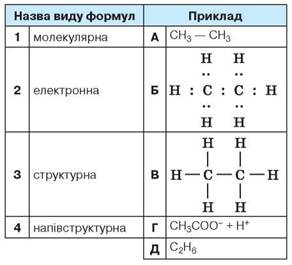
2. Установіть відповідність між видом формули речовини та наведеним конкретним прикладом.
3. Зазначте характеристики гомологів метану.
- А мають однаковий кількісний склад
- Б мають однаковий якісний склад
- В мають різний кількісний склад
- Г подібні за хімічною будовою
- Д виявляють схожі хімічні властивості
4. Оберіть формули гомологів метану.
- А C2H4
- Б C6H14
- В C5H10
- Г C2H6
5. Розташуйте назви насичених вуглеводнів за збільшенням кількості атомів Карбону в молекулі.
- А декан
- Б етан
- В бутан
- Г гептан
6. Складіть рівняння реакцій горіння зазначених речовин.
- А метан
- Б етен
- В етанол
- Г гептан
У відповіді зазначте, у якому рівнянні реакції сума коефіцієнтів найбільша, а в якому — найменша.
7. Гомолог метану масою 11 г займає об'єм 5,6 л (н. у.). Установіть формулу сполуки.
8. Відносна густина насиченого вуглеводню за повітрям дорівнює 0,55. Установіть формулу цієї сполуки. Обчисліть у ній масову частку Карбону.
9. Обчисліть, де більше молекул — в етані масою 3 г чи метані об'ємом 2,24 л (н. у.).
10. Установіть відповідність між назвою органічної сполуки та групою атомів, наявною в її молекулі.

11. Установіть відповідність між назвою кислоти та її молекулярною формулою.
|
Назва кислоти |
Формула кислоти |
||
|
1 |
карбонатна |
А |
СН3СООН |
|
2 |
олеїнова |
Б |
С17Н35СООН |
|
3 |
етанова |
В |
С17Н33СООН |
|
4 |
стеаринова |
Г |
Н2СО3 |
|
Д |
С16Н31СООН |
||
12. Гідрування етену відбувається за схемою C2H4 + H2 → C2H6. Визначте об’ємний склад суміші етену з воднем, якщо об’єм суміші після реакції зменшився на 20 л і залишилося 4 л водню. Об’єми газів виміряно за однакових умов.
13. Який об'єм хлору (н. у.) приєднався до етину, якщо маса утвореного продукту дорівнює 33,6 г?
14. Оберіть речовину, з якою не реагує етанова кислота.
- А магній
- Б магній оксид
- В калій гідроксид
- Г метан
15. Обчисліть масові частки та відношення мас елементів у аміноетановій кислоті.
16. Об'єм води, якою розбавляють 200 г розчину з масовою часткою сахарози 50 % та одержують новий розчин з масовою часткою цієї сполуки 20 %, дорівнює...
- А 50 мл
- Б 100 мл
- В 300 мл
- Г 200 мл
17. Який об'єм води необхідно випарувати з розчину масою 300 г і масовою часткою сахарози 20 %, щоб утворився розчин з масовою часткою 25 %?
18. Де більше атомів Карбону: у порції етанової кислоти масою 90 г чи в порції глюкози масою 90 г?
19. Однаковою чи різною буде масова частка розчиненої речовини в таких розчинах:
- а) виготовленому з 0,25 моль глюкози і 255 мл води;
- б) виготовленому з 0,5 моль метанолу і 84 мл води?
20. Двовалентний метал масою 6 г витіснив з етанової кислоти водень об'ємом 5,6 л (н. у.). Визначте назву цього металу й обчисліть масу розчину етанової кислоти з масовою часткою розчиненої речовини 10 %, що прореагував.
21. Добова норма вуглеводів 4-5 г на 1 кг маси тіла людини. Визначте об'єм вуглекислого газу, що утворюється внаслідок окиснення добової порції глюкози у вашому організмі.
Цей контент створено завдяки Міністерству освіти і науки України
